KI-gestütztes Unternehmen Lösungen für jeden Pharma-Workflow
Umfassende Suite validierter Softwarelösungen für Pharma-, Biotech- und Biowissenschaftsunternehmen.
Low-Code-aPaaS für Biowissenschaften – Einheitliche Integrationsarchitektur
Die Module von AmpleLogic arbeiten nicht in Silos. Jede Lösung ist miteinander verbunden – sie tauscht Daten aus, löst Arbeitsabläufe aus und sorgt für die Aufrechterhaltung einer einzigen Informationsquelle für alle Funktionen des Qualitäts-, Fertigungs- und Qualitätskontrolllabors.
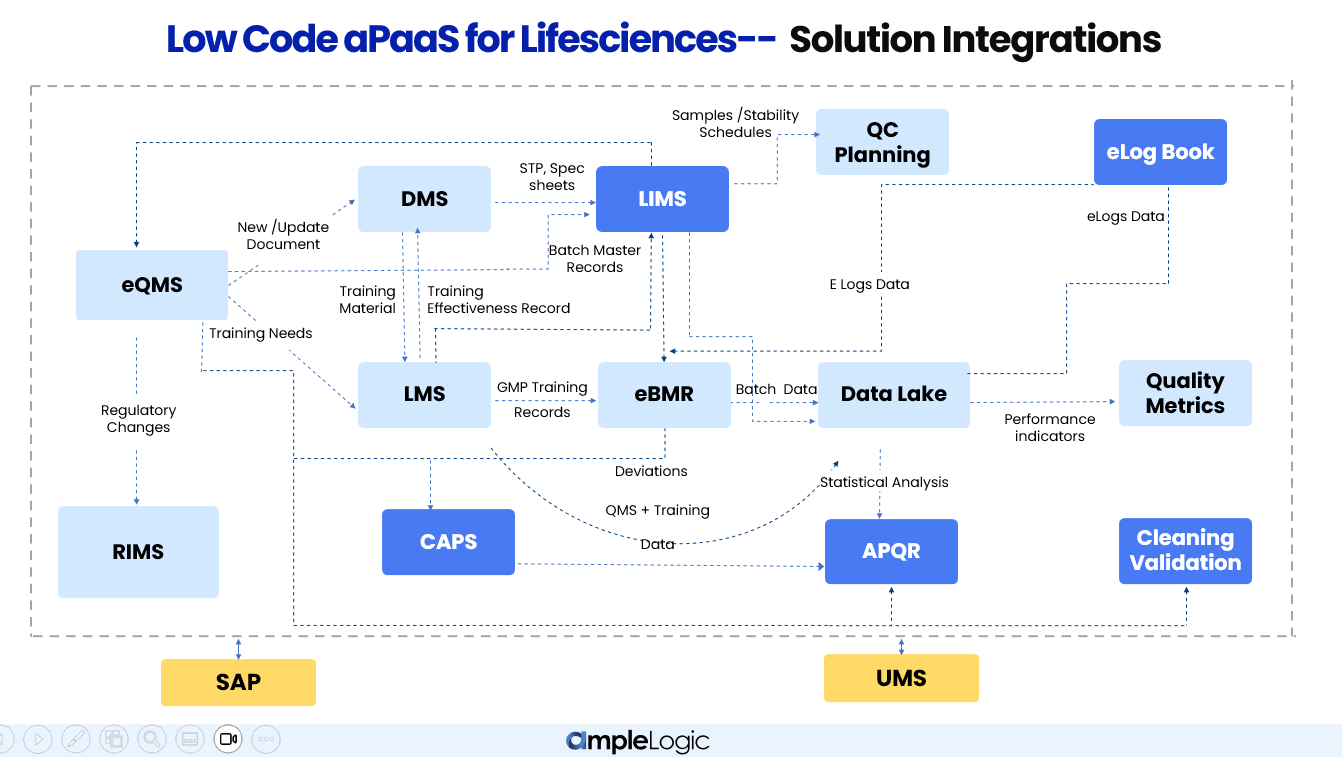
Wie AmpleLogic-Module in die Laborfunktionen Qualität, Fertigung und Qualitätskontrolle in Pharmaunternehmen integriert werden
Einheitlicher Data Lake
Alle Module werden in einen zentralen Data Lake eingespeist und ermöglichen Echtzeit-Leistungsindikatoren, Qualitätsmetriken und funktionsübergreifende Analysen ohne manuelle Datenkonsolidierung.
Automatisierte Workflow-Kaskaden
Ein einzelnes Ereignis – beispielsweise eine Abweichung in der Fertigung – löst automatisch CAPA in eQMS, eine Dokumentenüberarbeitung in DMS, eine Umschulung in LMS und eine Folgenabschätzung in APQR aus.
Bidirektionaler Datenfluss
Der Datenfluss zwischen Modulen erfolgt in beide Richtungen. Beispielsweise sendet LMS Aufzeichnungen über die Wirksamkeit von Schulungen zurück an eQMS, und LIMS sendet Analyseergebnisse zur Chargenfreigabe an eBMR zurück.
Wie funktionsübergreifende Integrationen funktionieren
Qualitätsmanagement
Das Qualitätsmanagement-Ökosystem stellt sicher, dass jede Abweichung, CAPA, Änderungskontrolle und Auditfeststellung durchgängig verfolgt wird. eQMS steht im Mittelpunkt – es löst Dokumenten-Workflows im DMS aus, Schulungsaufgaben im LMS und speist statistische Daten in APQR für jährliche Produktqualitätsüberprüfungen ein.
Neues/aktualisiertes Dokument
Wenn im eQMS eine Abweichung oder Änderungskontrolle auftritt, initiiert das DMS automatisch einen SOP-Überarbeitungsworkflow und stellt so sicher, dass die Dokumente bei jedem Qualitätsereignis aktuell bleiben.
Schulungsbedarf
Neue oder überarbeitete SOPs lösen automatische Schulungszuweisungen im LMS aus. Aufzeichnungen über die Wirksamkeit von Schulungen fließen zurück an eQMS, um den Qualitätskreislauf zu schließen.
Statistische Analyse
Chargendaten, Abweichungen, CAPA-Aufzeichnungen und Prozessparameter werden im Data Lake aggregiert und für umfassende jährliche Produktqualitätsprüfungen in APQR eingespeist.
QMS + Schulungsdaten
Kalibrierungsabweichungen und vorbeugende Wartungsaufzeichnungen von CAPS fließen in APQR ein und liefern ein vollständiges Bild der Auswirkungen von Geräten und Instrumenten auf die Produktqualität.
Bleiben Sie in den Biowissenschaften an der Spitze
Erhalten Sie die neuesten Produktaktualisierungen, Compliance-News und Brancheneinblicke in Ihren Posteingang.