Realice un seguimiento de cada envío y registro a nivel mundial
Sistema de gestión de información reglamentaria especialmente diseñado para productos farmacéuticos: automatice los envíos, realice un seguimiento de las presentaciones ante ANDA y DMF y gestione los ciclos de vida de los productos farmacéuticos en más de 120 países con software de cumplimiento normativo impulsado por IA.
120+
Países admitidos
50%
Envíos más rápidos
100%
Listo para auditoría
24/7
Monitoreo de cumplimiento
Desafíos de RIMS: por qué la gestión regulatoria manual se queda corta
Desafíos críticos que obstaculizan el cumplimiento, las presentaciones y el acceso al mercado
Regulaciones globales en constante evolución
Mantenerse al día con la FDA, la EMA, la MHRA, la CDSCO, la OMS, Health Canada, TGA y más de 100 autoridades regionales exige una vigilancia continua y una adaptación rápida.
Datos regulatorios fragmentados
La información regulatoria crítica dispersa en correos electrónicos, hojas de cálculo, unidades compartidas y sistemas heredados crea puntos ciegos y brechas de cumplimiento.
Formatos de envío complejos
La gestión de eCTD, ACTD, NeeS y presentaciones en papel en diferentes regiones requiere experiencia especializada y una coordinación manual propensa a errores.
Mala visibilidad y seguimiento
No hay un panel unificado para el estado en tiempo real de los envíos, aprobaciones, consultas y cronogramas de renovación globales en todos los mercados.
Procesos manuales y propensos a errores
La gran dependencia de la comunicación por correo electrónico, la entrada manual de datos y las hojas de cálculo desconectadas aumenta el riesgo de incumplimiento de plazos y sanciones regulatorias.
Desafíos de integración
Los sistemas QMS, DMS, ERP y de seguridad desconectados provocan duplicación de datos, inconsistencias y flujos de trabajo regulatorios multifuncionales lentos.
Problemas de escalabilidad
Las crecientes carteras de productos en todas las geografías aumentan exponencialmente la complejidad regulatoria, abrumando los enfoques de seguimiento manual.
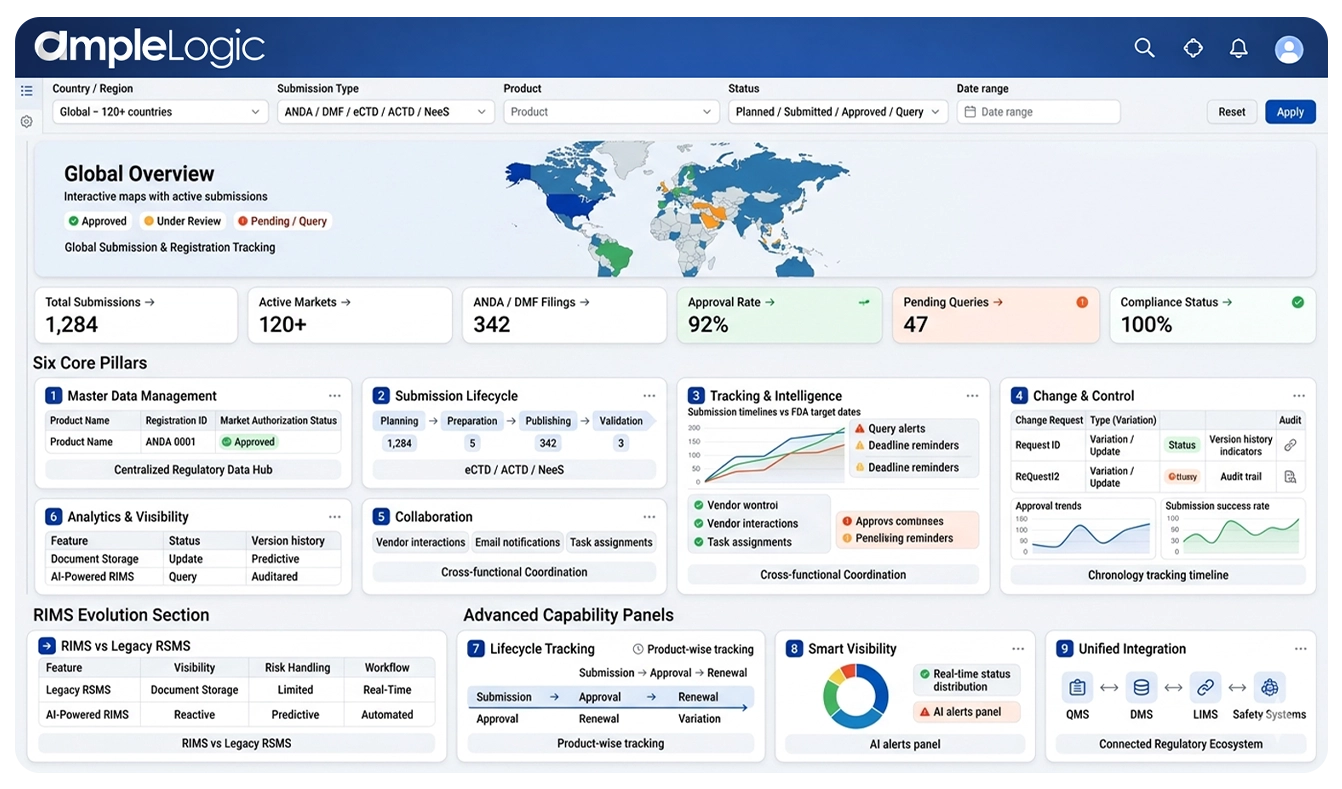
Descripción general del software AmpleLogic RIMS
Seis pilares que permiten la gestión integral del ciclo de vida regulatorio
Gestión de datos maestros
Registro centralizado de productos, autorización de mercado global y seguimiento del ciclo de vida en todas las autoridades reguladoras.
Ciclo de vida de envío
Flujos de trabajo automatizados para planificación, preparación, publicación y validación de envíos de eCTD, ACTD y NeeS con seguimiento de ANDA y DMF.
Seguimiento e inteligencia
Estado de envío en tiempo real, gestión de consultas y aprobaciones, fechas objetivo de la FDA y seguimiento proactivo de los plazos en todos los mercados.
Cambio y control
Control de cambios, gestión de variaciones y proceso de mejora continua (CIP) con seguimientos de auditoría completos e historial de versiones.
Colaboración
Coordinación de proveedores, notificación al cliente y alertas automáticas por correo electrónico para flujos de trabajo regulatorios multifuncionales sin interrupciones.
Análisis y visibilidad
Paneles gráficos, seguimiento cronológico, análisis del ciclo de vida e inteligencia lista para el cumplimiento para tomar decisiones regulatorias informadas.
RIMS: La próxima evolución de RSMS
Si bien las plataformas RSMS heredadas eran almacenes de documentos pasivos, RIMS es un ecosistema de gestión regulatoria inteligente impulsado por IA que impulsa activamente el cumplimiento, predice riesgos y acelera el tiempo de comercialización.
Gestión de datos
Complete el registro de productos y los datos regulatorios globales en un sistema centralizado con control de datos maestros y seguimiento del ciclo de vida.
Seguimiento del ciclo de vida
Monitorear aprobaciones, variaciones y renovaciones para garantizar el cumplimiento normativo continuo en todos los mercados.
Visibilidad inteligente
Visibilidad global en tiempo real y monitoreo proactivo a través de alertas inteligentes y paneles de cumplimiento.
Integración unificada
Integración perfecta con QMS, DMS, LIMS y sistemas de seguridad para construir un ecosistema de gestión regulatoria unificado.
Módulos de flujo de trabajo de RIMS: gestión del ciclo de vida de envío
Ocho módulos interconectados que guían los procesos regulatorios desde la estrategia hasta el cumplimiento continuo
Fundación de datos regulatorios
Configuración del mercado global y repositorio de datos maestros para DMF, CEP, LOA y seguimiento del ciclo de vida del producto en todas las autoridades.
Planificación de envío
Desarrollo de estrategias, gestión de cronogramas, seguimiento de hitos y asignación de recursos para presentaciones regulatorias globales.
Preparación de la presentación
Compilación de expedientes, control de versiones y ensamblaje de documentos para la preparación de eCTD/ACTD/NeeS con comprobaciones de validación automatizadas.
Ejecución de envío
Validación, publicación para las autoridades sanitarias, envío de portales, seguimiento de ANDA y seguimiento del estado de las autoridades en tiempo real.
Gestión de revisiones
Seguimiento de consultas, gestión de deficiencias, registros de comunicación de autoridades y seguimiento del cronograma de respuesta en todos los mercados.
Gestión del ciclo de vida de los productos farmacéuticos
Variaciones, renovaciones, cambios posteriores a la aprobación y actualizaciones de etiquetas con seguimiento completo del ciclo de vida y alertas automatizadas.
Monitoreo de cumplimiento
Alertas automatizadas, seguimiento de compromisos, preparación para inspecciones e inteligencia proactiva sobre cambios regulatorios.
Análisis e informes
Paneles de control en tiempo real, informes gráficos, información sobre envíos globales y análisis específicos de GDUFA/autoridad.

Orquestación de un extremo a otro
Cada módulo de flujo de trabajo se integra perfectamente con QMS, DMS, LIMS y sistemas de seguridad, eliminando silos de datos y transferencias manuales durante todo el ciclo de vida regulatorio.
Características clave del software AmpleLogic RIMS
Doce capacidades críticas que permiten la excelencia regulatoria
Seguimiento del registro de productos
Realice un seguimiento de los registros de productos en más de 120 países con actualizaciones de estado automatizadas, alertas de fechas límite y gestión completa del ciclo de vida de los productos farmacéuticos.
Preparación y publicación de envíos
Monitoreo de aprobación y rechazo
Rastreador de ANDA y fechas objetivo de la FDA
Seguimiento DMF y control de cambios
Gestión de compromisos y variaciones
Gestión de proveedores y partes interesadas
Informes gráficos y paneles
Flujos de trabajo regulatorios farmacéuticos automatizados
Firmas electrónicas y pistas de auditoría
Repositorio de documentos centralizado
Motor de validación de envío
RIMS impulsado por IA: análisis regulatorio inteligente
Seis capacidades impulsadas por IA que aceleran los flujos de trabajo regulatorios y reducen el riesgo
Seguimiento del cumplimiento de la IA
Supervisa y se adapta continuamente a los estándares regulatorios locales y globales en evolución, actualizando automáticamente los procesos para garantizar el cumplimiento sin intervención manual.
Análisis predictivo
Analiza datos históricos y en tiempo real para identificar riesgos potenciales y brechas de cumplimiento antes de que aumenten, lo que ayuda a mitigar problemas de manera proactiva y evitar sanciones.
Informes automatizados
La IA automatiza la generación de informes y documentación regulatorios, garantizando que sean precisos, oportunos y estén listos para auditorías con una mínima participación humana.
Motor de mitigación de riesgos
Los algoritmos impulsados por IA evalúan patrones de datos para señalar posibles riesgos de cumplimiento, ofreciendo información predictiva y recomendando acciones correctivas.
Inteligencia de cambio regulatorio
Realiza un seguimiento y procesa los cambios regulatorios en tiempo real, implementándolos automáticamente en sus sistemas para garantizar el cumplimiento continuo de los últimos estándares.
Optimización del flujo de trabajo
La IA optimiza los flujos de trabajo, minimiza los costos operativos, acelera los procesos regulatorios y garantiza un cumplimiento consistente en todos los niveles comerciales.
Seguidores regulatorios globales: FDA, EMA y monitoreo de RoW
Tres módulos de seguimiento regionales para una autorización de mercado integral
Rastreador regulatorio de la FDA de EE. UU.
Rastreador ANDA y rastreador DMF con hitos del ciclo de vida de la FDA que incluyen fechas de acción objetivo de IND, NDA, ANDA, BLA, tarifas de GDUFA y presentaciones 505(b)(2).
Seguimiento regulatorio de la UE y el Reino Unido
Administre los procedimientos de EMA y MHRA, las variaciones centralizadas/descentralizadas/de reconocimiento mutuo, los cronogramas de PSUR y las presentaciones del Reino Unido posteriores al Brexit con flujos de trabajo automatizados.
Rastreador regulatorio global del derecho de vía
Optimice las presentaciones de APAC, LATAM, MENA y África con un seguimiento del ciclo de vida específico de cada país para Health Canada, TGA, CDSCO, WHO PQ y más de 100 autoridades.
Cumplimiento de RIMS: estándares regulatorios globales
Soporte total para marcos regulatorios globales y estándares de cumplimiento.
Apoyo a las principales autoridades
Cobertura completa para la FDA de EE. UU., EMA, MHRA, OMS, Health Canada, TGA, CDSCO, ANVISA, PMDA y más de 100 autoridades sanitarias mundiales.
Gestión de formatos multirregionales
Soporte nativo para eCTD, ACTD, NeeS y formatos en papel con monitoreo de renovación automatizado y validación específica del formato.
21 CFR Parte 11 y Anexo 11 de la UE
Controles totalmente compatibles que incluyen firmas electrónicas, pistas de auditoría, salvaguardias de integridad de datos y control de versiones seguro.
Monitoreo proactivo y alertas
Alertas automatizadas de plazos, fechas de vencimiento de compromisos, ventanas de renovación y cambios regulatorios con reducción de riesgos en tiempo real.
Preparación IDMP
Admite los estándares ISO IDMP para sustancias, productos, organizaciones y datos referenciales para prepararse para los requisitos de identificación de la EMA.
Listo para ICH eCTD 4.0
Preparado para el futuro para el modelo de datos eCTD 4.0 de próxima generación con capacidades de planificación de contenido estructurado, gestión de metadatos y envío de autoridades.
AmpleLogic RIMS frente a los competidores
Cómo AmpleLogic supera a los RIMS heredados y las soluciones puntuales
| Capacidad | LLANTAS AmpleLogic | Competidoras |
|---|---|---|
| Arquitectura | Código bajo/sin código en aPaaS unificada | Arquitectura rígida, se necesita mucha personalización |
| Enfoque de datos | Repositorio unificado de datos maestros | Datos fragmentados en módulos y silos |
| Cobertura del ciclo de vida | De principio a fin (desde la planificación hasta el seguimiento posterior a la aprobación) | A menudo requiere módulos adicionales separados |
| Integración | Sin interrupciones (QMS, DMS, ERP, seguridad, LIMS) | Independiente, alto costo y esfuerzo de integración |
| Automatización e IA | Alertas impulsadas por IA, análisis predictivos e informes automáticos | Automatización limitada, flujos de trabajo manuales estáticos |
| Costo total de propiedad | Menor coste total de propiedad, implementación rápida y pago a medida que crece | Altas tarifas de licencia y costos de mantenimiento continuos |
| Velocidad de implementación | Semanas con plantillas prevalidadas | Meses a años de implementación. |
| Preparación para el eCTD 4.0 | Preparado para el futuro con un modelo de datos estructurados | Cronograma incierto y dependiente de la hoja de ruta |
Integraciones empresariales de RIMS
Diez módulos de integración que conectan sistemas regulatorios, de calidad y de fabricación.
eQMS
Control de cambios bidireccional, CAPA y enlace de desviación
DMS
Documentos reglamentarios y SOP con control de versión
LMS
Registros de formación y gestión de competencias.
LIMAS
Datos analíticos e integración de CoA para presentaciones
libro de registro electrónico
Datos del libro de registro de GxP vinculados a registros regulatorios
eBMR/MES
Datos de registro de lotes para presentaciones regulatorias
CVS
Datos de validación de limpieza para presentaciones regulatorias
GORRAS
Registros de calibración de equipos para cumplimiento
SAP/Oracle
Sincronización de datos maestros de materiales y cadena de suministro
FOTOVOLTAICA
Datos de eventos adversos e integración PSUR/PBRER
ROI de RIMS: impacto regulatorio mensurable
Impacto cuantificado de la gestión del ciclo de vida regulatorio asistida por IA
Preparación de la presentación
50-60% más rápidoProceso manual
8-12 semanas
Con llantas AmpleLogic
3-5 semanas
Entrada de datos regulatorios
75% de reducciónProceso manual
40+ horas/semana
Con llantas AmpleLogic
8-10 horas/semana
Cumplimiento de plazos
Plazos incumplidos casi a ceroProceso manual
85-90% a tiempo
Con llantas AmpleLogic
99%+ a tiempo
Tiempo de respuesta a la consulta
Respuesta un 70% más rápidaProceso manual
5-10 días hábiles
Con llantas AmpleLogic
1-3 días hábiles
Preparación de auditoría
90% de ahorro de tiempoProceso manual
2-4 semanas
Con llantas AmpleLogic
Horas (siempre listas)
Generación de informes
95% más rápidaProceso manual
3-5 días por informe
Con llantas AmpleLogic
Minutos (generados automáticamente)
Destacado en el Informe Gartner
AmpleLogic RIMS ha sido reconocido como proveedor representativo en la Guía de mercado de Gartner® para soluciones de gestión de información regulatoria de ciencias biológicas, septiembre de 2024 (ID G00769345).
Industrias atendidas por AmpleLogic RIMS
Ocho verticales de la industria que aprovechan AmpleLogic RIMS para lograr excelencia regulatoria
Productos farmacéuticos
Software regulatorio compatible con GMP para registro de medicamentos, presentaciones de NDA/ANDA y autorización de mercado global con gestión del ciclo de vida completo
Biotecnología
Presentaciones de BLA, registros de biosimilares y gestión compleja del ciclo de vida de productos biológicos
Dispositivos médicos
510(k), PMA, marcado CE, presentaciones EUDAMED/UDI y gestión de clasificación de dispositivos
Terapia genética
Presentaciones IND/BLA para terapias avanzadas con seguimiento de vías regulatorias especializadas
Fabricantes de API
Rastreador DMF para aplicaciones CEP y registro API global entre autoridades
Alimentos y bebidas
Registros de aditivos alimentarios, solicitudes de nuevos alimentos y presentaciones de declaraciones de propiedades saludables
Cannabis y tabaco
Seguimiento regulatorio especializado para solicitudes de licencias de cannabis y presentaciones de productos de tabaco
Productos cosméticos
Notificaciones de productos cosméticos, registros CPNP/FDA y seguimiento del cumplimiento de ingredientes
¿Listo para transformar sus operaciones regulatorias?
Reemplace las hojas de cálculo fragmentadas y el seguimiento manual con inteligencia regulatoria lista para auditorías y basada en IA.
Manténgase a la vanguardia en las ciencias biológicas
Reciba las últimas actualizaciones de productos, noticias sobre cumplimiento y conocimientos de la industria en su bandeja de entrada.