Administre estudios de estabilidad de principio a fin dentro de su LIMS
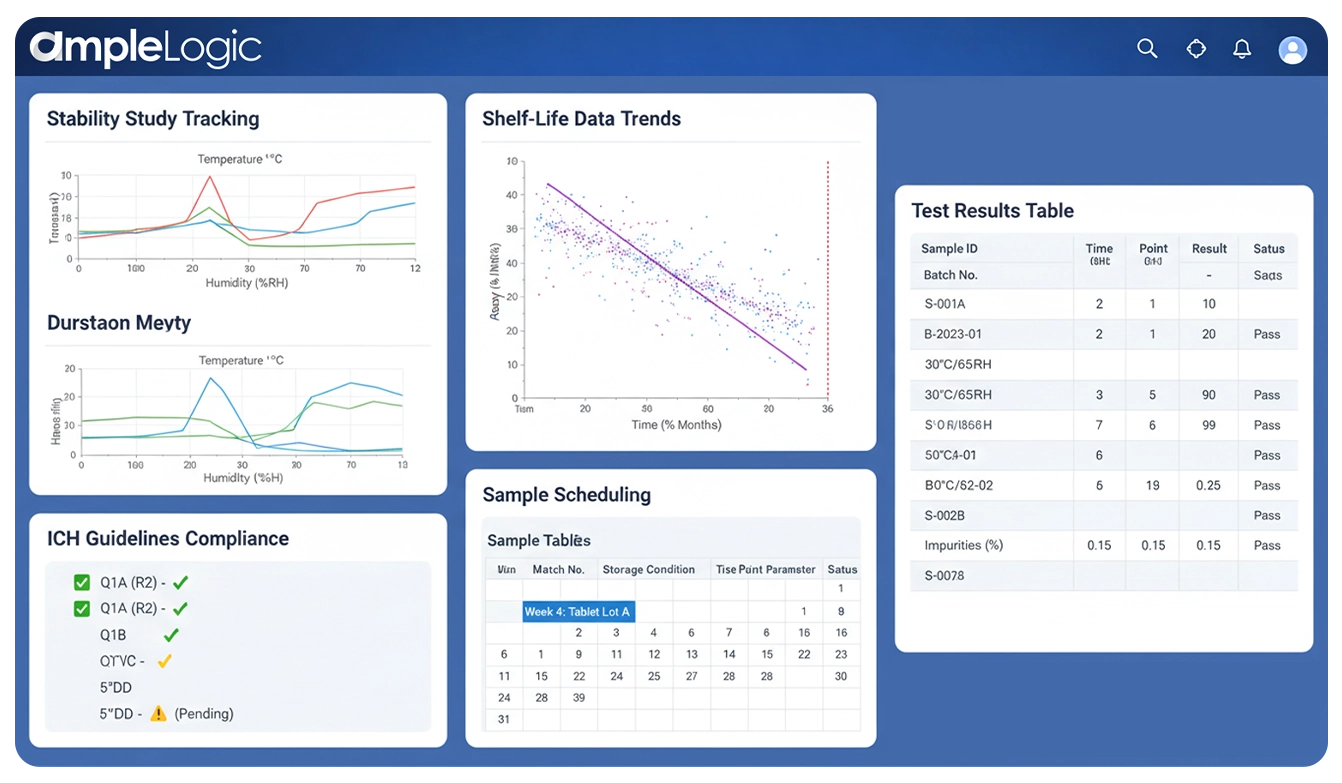
AmpleLogic ofrece gestión integral del cronograma de estabilidad, desde la creación del protocolo de pruebas de estabilidad y la planificación del calendario del cronograma de estabilidad hasta el monitoreo de la cámara, la ejecución de pruebas, el análisis de tendencias, la determinación de la vida útil y la generación de informes listos para la regulación alineados con los requisitos de ICH Q1A, FDA y GMP.
40%
Configuración de estudio más rápida
100%
Cumplimiento de la PCI
30%
Reducción de tirones perdidos
60%
Menos seguimiento manual
50%
Ahorro de costos
3–6
Mes de implementación
¿Qué es la gestión del cronograma de estabilidad?
La gestión del cronograma de estabilidad es la planificación, ejecución y seguimiento sistemáticos de estudios de estabilidad farmacéutica. Garantiza que cada lote de producto se someta a las condiciones de almacenamiento, tiempos de muestreo y pruebas analíticas correctas según lo definido por el protocolo de prueba de estabilidad, lo que permite una determinación precisa de la vida útil y el cumplimiento normativo de ICH Q1A, FDA 21 CFR Parte 211.166 y requisitos GMP.
Protocolo de prueba de estabilidad
Un protocolo de prueba de estabilidad define el diseño del estudio: condiciones de almacenamiento, momentos temporales, parámetros de prueba, criterios de aceptación y configuraciones de embalaje. AmpleLogic automatiza la creación de protocolos con plantillas compatibles con ICH Q1A.
Calendario de Estabilidad
El calendario del cronograma de estabilidad es una línea de tiempo visual de todas las fechas de extracción, asignaciones de cámaras y asignaciones de analistas en cada estudio activo. AmpleLogic genera automáticamente y mantiene este calendario en tiempo real.
Gestión del cronograma de estabilidad
La gestión del cronograma de estabilidad coordina todo el ciclo de vida, desde la aprobación del protocolo hasta la extracción de muestras, la ejecución de pruebas, el análisis de tendencias y la determinación de la vida útil, en una única plataforma validada.
Desafíos en la gestión de cronogramas de estabilidad sin automatización
Las organizaciones que dependen de procesos manuales para la gestión de protocolos de pruebas de estabilidad y el seguimiento del calendario de programación de estabilidad enfrentan riesgos críticos.
Gestión manual del cronograma de estabilidad
Los equipos dependen de hojas de cálculo y registros en papel para planificar cronogramas de estabilidad, lo que genera puntos de atracción perdidos, conflictos de programación y falta de visibilidad en tiempo real de los cronogramas de los estudios.
Protocolos de prueba de estabilidad inconsistentes
Sin un sistema estandarizado, la creación de protocolos de prueba de estabilidad varía entre equipos y sitios, lo que genera lagunas regulatorias, hallazgos de auditoría y diseños de estudios inconsistentes.
Sin calendario de programación de estabilidad centralizado
La ausencia de un calendario unificado de estabilidad significa que los analistas no pueden ver los próximos retiros, asignaciones de cámaras o estudios superpuestos en un solo lugar.
Datos ambientales desconectados
Los datos de temperatura y humedad de la cámara se rastrean por separado de los estudios de estabilidad, lo que crea brechas de trazabilidad y una respuesta de excursión retardada.
Análisis e informes de tendencias retrasados
La recopilación manual de datos para el análisis de tendencias de estabilidad retrasa la determinación de la vida útil, las presentaciones regulatorias y los cronogramas de lanzamiento de productos.
Riesgo de cumplimiento de sistemas fragmentados
El uso de múltiples herramientas desconectadas para la gestión del programa de estabilidad aumenta los riesgos de integridad de los datos y dificulta la preparación para las auditorías ICH Q1A y FDA.
Enfoque AmpleLogic para el protocolo de pruebas de estabilidad y la automatización de horarios
Seis pasos integrados que transforman la gestión manual del cronograma de estabilidad en un flujo de trabajo totalmente automatizado y compatible con ICH.
Definir protocolo de prueba de estabilidad
Cree protocolos de prueba de estabilidad que cumplan con ICH Q1A con diseños de estudio configurables, condiciones de almacenamiento, criterios de aceptación y programas de muestreo automatizados, todo en un único sistema validado.
Calendario de programación de estabilidad de construcción
Genere automáticamente un calendario visual de estabilidad con fechas de extracción de puntos temporales, asignaciones de cámaras, asignación de analistas y recordatorios automáticos, eliminando por completo la planificación manual.
Monitorear las condiciones de la cámara
Monitoreo de temperatura y humedad en tiempo real con alertas de excursión automatizadas, integración de sensores y datos ambientales vinculados directamente a registros de estudios de estabilidad.
Ejecutar y capturar resultados
Ejecute pruebas analíticas dentro del flujo de trabajo LIMS integrado con conectividad directa de instrumentos, cálculos en línea y trazabilidad completa desde la muestra hasta el resultado.
Analice tendencias y determine la vida útil
Análisis de tendencias de estabilidad impulsado por IA con modelado de degradación, proyección estadística de vida útil, determinación de caducidad e informes de intervalos de confianza.
Generar informes regulatorios
Produzca automáticamente informes de estabilidad que cumplan con ICH, paquetes de envío a la FDA y documentación del programa de estabilidad GMP a partir de sus datos de estabilidad.
Centro de datos y calendario de programación de estabilidad de AmpleLogic
Una plataforma centralizada que unifica la gestión del protocolo de pruebas de estabilidad, el calendario de programación de estabilidad, el análisis de tendencias y la documentación de cumplimiento en un solo lugar.
Panel de estudio unificado
Vista única de todos los estudios de estabilidad activos, completados y planificados con estado en tiempo real, próximas fechas de extracción y alertas vencidas en cada producto y condición.
Motor de gestión de programación de estabilidad
Gestión centralizada de la programación de estabilidad con programación de extracción automatizada, reprogramación dinámica, gestión de colas basada en prioridades y vistas basadas en calendario para cada estudio.
Análisis de tendencias interactivo
Gráficos de superposición de lotes múltiples, ajuste de curvas de degradación, detección OOT/OOS y pronóstico predictivo de vida útil, todo accesible desde una única consola de análisis.
Seguimiento de auditoría completo
Cada acción, desde la creación del protocolo de prueba de estabilidad hasta el ingreso de resultados y la generación de informes, se captura con registros de auditoría con marca de tiempo, identificados por el usuario y que cumplen con ALCOA+.
Centro de notificaciones inteligente
Alertas configurables para próximas extracciones, pruebas atrasadas, resultados de OOT, excursiones de cámara y desviaciones de protocolo con flujos de trabajo de escalada de varios niveles.
Integración entre sistemas
Integración bidireccional con LIMS, ERP, QMS y sistemas de instrumentos para crear una única fuente de verdad para todos los datos de estabilidad en toda su organización.
Gestión de programas de estabilidad manual versus automatizada
Vea cómo AmpleLogic transforma todos los aspectos de la gestión del protocolo de pruebas de estabilidad y las operaciones del calendario del cronograma de estabilidad.
| Área | Antes (manual) | Después (AmpleLogic) |
|---|---|---|
| Programación de estudios | Seguimiento manual de hojas de cálculo, conflictos de programación | Calendario de estabilidad automatizado con recordatorios |
| Creación de protocolo | Documentos de Word, formatos inconsistentes en todos los sitios. | Plantillas de protocolos de pruebas de estabilidad estandarizadas (ICH Q1A) |
| Gestión de extracción | Tirones perdidos, sin visibilidad en tiempo real | Cero tirones perdidos con programación automática y alertas |
| Monitoreo de cámara | Sensores desconectados, respuesta de excursión retrasada | Monitoreo en tiempo real con alertas instantáneas |
| Análisis de tendencias | Gráficos manuales de Excel, semanas para compilar | Análisis impulsado por IA, proyección instantánea de la vida útil |
| Informes | Compilación manual, propensa a errores | Informes listos para la normativa ICH/FDA con un solo clic |
| Preparación para la auditoría | Lucha por reunir pruebas | Siempre listo para auditorías con seguimiento ALCOA+ completo |
Confiable en todas las ciencias biológicas
Cumplimiento normativo para el protocolo de pruebas de estabilidad y la gestión del cronograma
¿Listo para automatizar la gestión de su cronograma de estabilidad?
Vea cómo AmpleLogic transforma la creación de protocolos de pruebas de estabilidad, la planificación del calendario de programación de estabilidad y la determinación de la vida útil en un único flujo de trabajo automatizado que cumple con ICH.
Manténgase a la vanguardia en las ciencias biológicas
Reciba las últimas actualizaciones de productos, noticias sobre cumplimiento y conocimientos de la industria en su bandeja de entrada.