Verwalten Sie jedes Qualitätsereignis in einem integrierten eQMS
AmpleLogic bietet eine cloudbasierte, KI-gestützte pharmazeutische QMS-Softwareplattform, die für Compliance auf Unternehmensniveau entwickelt wurde. Unsere digitale QMS-Plattform vereint CAPA-Management, Abweichungsmanagement, Änderungskontrolle, Audits und Lieferantenqualität in einer GxP-konformen Softwarelösung für das Qualitätsereignismanagement – der Pharma-, Biotech- und Medizingeräteunternehmen weltweit vertrauen.
11+
Integrierte QMS-Module
100 %
Konform mit 21 CFR Teil 11
50 %
Schnellerer CAPA-Abschluss
300+
Globale Implementierungen
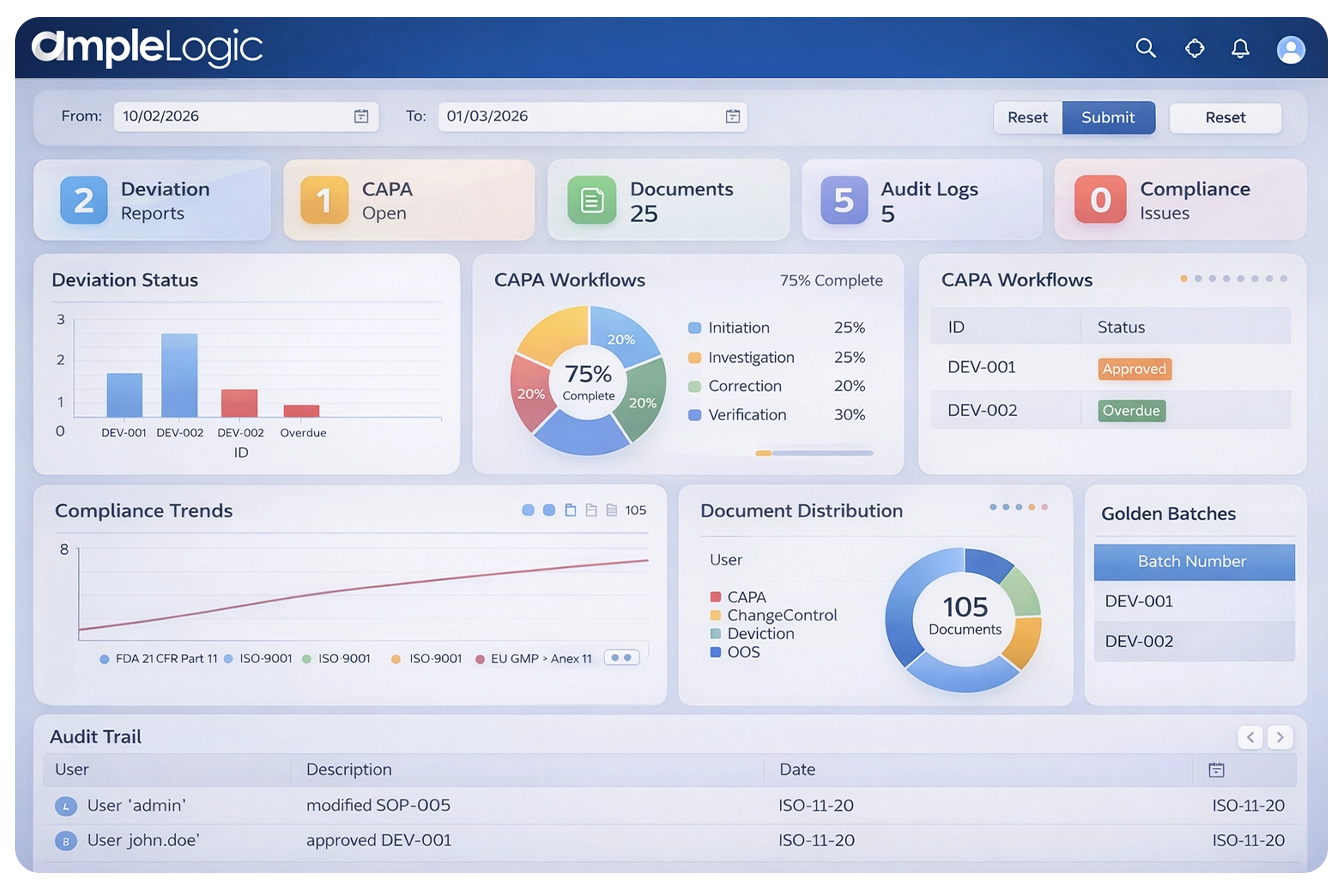
Warum veraltete Qualitätsmanagementsystem-Software unzureichend ist
Wie fragmentierte manuelle Prozesse in pharmazeutischer Compliance-Management-Software und veralteten GMP-Qualitätsmanagementsystemen zu Verzögerungen bei Qualitätsereignissen, Softwarelücken bei der Nichtkonformitätsverwaltung und höheren Qualitätskosten führen
Nichteinhaltung von Vorschriften
Hohes Risiko von Strafen aufgrund manueller Dokumentationsfehler, fehlender Audit-Trails und eingeschränkter Rückverfolgbarkeit – Probleme, die durch eine GxP-konforme Qualitätsmanagementsystem-Software beseitigt werden
Isolierte Qualitätssysteme
Eigenständige QMS-Module mit schwachen Integrationen führen zu verzögerten Untersuchungen, doppelter Dateneingabe und längeren CAPA-Abschlüssen im gesamten Qualitätsmanagementsystem des Unternehmens
Keine Echtzeitanalyse
Das Fehlen von Dashboards für Abweichungsmanagement, CAPA, Änderungskontrolle und OOS schränkt die proaktive Entscheidungsfindung und Risikotransparenz ohne eine digitale Qualitätsmanagementplattform ein
Langsame Untersuchungszyklen
Papierbasierte oder E-Mail-gesteuerte Untersuchungen dauern zwei- bis viermal länger als digitale Arbeitsabläufe in moderner pharmazeutischer Qualitätsmanagementsoftware und verzögern die Chargenfreigabe
Begrenzte externe Zusammenarbeit
Kein Partnerzugriff in Echtzeit für Lieferantenqualitätsmanagement, CDMO-Untersuchungen oder Vertragslaborkoordination – eine Lücke, die cloudbasierte QMS-Software schließt
Globale Ausrichtungslücken
Betriebe mit mehreren Standorten kämpfen mit inkonsistenten Prozessen, fragmentierten Daten und der Unfähigkeit, Qualitätsmetriken ohne ein unternehmensweites Qualitätsmanagementsystem zu konsolidieren

Die Kosten, manuell zu bleiben
Unternehmensqualitätsmanagementsystem – Vorteile
Cloudbasierte SaaS-QMS-Plattform mit Lebenszykluskontrolle, Einhaltung gesetzlicher Vorschriften, Automatisierung von Qualitätsworkflows und validierter Unternehmensqualitätsplattform für Pharma und Biotechnologie
Wirksamkeit im geschlossenen Regelkreis
Integrierte Verifizierung für CAPA-Management, Änderungskontrolle, Abweichungen und Audit-Management-Software-Workflows
Echte End-to-End-Rückverfolgbarkeit
Verknüpfung von Abweichungsmanagement, CAPA, Änderungen, Beschwerden, OOS/OOT und Audit-Datensätzen mit einem Klick in einem einheitlichen QMS
Jederzeit revisionssicher
Automatisierte Beweiszusammenstellung, unveränderliche Prüfprotokolle und Inspektions-Dashboards für FDA 21 CFR Part 11-konforme QMS-Abläufe
Risikobasierte Entscheidungsunterstützung
Priorisieren Sie Maßnahmen mithilfe der Risikobewertung und historischen Qualitätsdaten innerhalb des Qualitätsmanagementsystems des Unternehmens
KI-gestützte Qualitätsintelligenz
Schnellere RCA, Anomalieerkennung und Wirksamkeitsüberprüfung mit KI-gestützten Funktionen des Qualitätsmanagementsystems
Automatisierte Eskalation und Erinnerungen
Risiko- und zeitgesteuerte Erinnerungen mit automatischer Eskalation in der Pharma-Compliance-Management-Software
Warum AmpleLogic – Cloud-QMS-Software für Biowissenschaften
Branchenführende Software für das pharmazeutische Qualitätsmanagement mit nachgewiesenem ROI und behördlicher Vertretbarkeit
Die Kosten manueller Qualität
Manuelle Qualitätsprozesse erhöhen Fehler, Verzögerungen und Betriebskosten – Cloud-QMS-Software beseitigt diese Ineffizienzen
Intelligente Empfehlungsmaschine
Intelligente, datengesteuerte Empfehlungen zur Beschleunigung der Problemlösung auf Ihrer digitalen Qualitätsmanagementplattform
Cloud-basierter aPaaS-Vorteil
Cloudbasierte QMS-Software mit geringem Code beschleunigt die Bereitstellung, Anpassung und den Rollout an mehreren Standorten für das pharmazeutische Qualitätsmanagement
GxP-Konformität und -Validierung
Ein GxP-konformes Qualitätsmanagementsystem mit integrierten FDA 21 CFR Part 11-Kontrollen stellt sicher, dass Prozesse den gesetzlichen Standards entsprechen und Audits bestehen
Quantifizierbare ROI-Kennzahlen
Misst Effizienzgewinne und Kosteneinsparungen durch den betriebsübergreifenden Einsatz von Software für das Qualitätsmanagementsystem von Unternehmen
Nahtlose Integrationen
Lässt sich mühelos mit LIMS, eBMR, DMS, ERP und vorhandener Qualitätsmanagementsystemsoftware in Ihrem Technologie-Stack verbinden
CAPA, Abweichung, Audit und Lieferantenqualitätsmanagement
Entdecken Sie jedes Modul unserer Qualitätsmanagementsystemsoftware – CAPA-Managementsoftware, Abweichungsmanagementsoftware, Änderungskontrollmanagementsoftware, Auditmanagementsoftware, Beschwerdemanagementsoftware, Qualitätsrisikomanagementsoftware, Lieferantenqualität und Nichtkonformitätsmanagement
Abweichungsmanagement
Pharmazeutisches Qualitätsereignismanagementsystem
Durchgängiges Abweichungslebenszyklusmanagement für die pharmazeutische Herstellung – von der Erkennung bis zum Abschluss mit vollständiger Rückverfolgbarkeit, risikobasierter Klassifizierung und GMP-Vertretbarkeit.
CAPA-Management
Pharmazeutische CAPA-Management-Software
Geschlossener Lebenszyklus von Korrektur- und Präventivmaßnahmen – von der Einleitung über die Ursachenforschung, die Automatisierung des Arbeitsablaufs bis hin zur Wirksamkeitsverfolgung mit FDA- und GxP-Konformität.
Änderungskontrolle
Planen, bewerten, implementieren, überprüfen
Verwalten Sie geplante und ungeplante Änderungen an Prozessen, Geräten, Materialien und Systemen mit strukturierter Auswirkungsanalyse, Genehmigung mehrerer Interessengruppen und Überprüfung nach der Implementierung.
Auditmanagement
Audit-Management-Software für pharmazeutische Qualitätssysteme
Internes, externes und Lieferantenauditmanagement mit automatisierter Planung, Terminierung, Integration von Erkenntnissen in CAPA und Dashboards zur Vorbereitung auf behördliche Inspektionen.
Beschwerdemanagement
KI-gestütztes Beschwerdemanagement für pharmazeutische Qualitätssysteme
Durchgängiger Beschwerdelebenszyklus von der Aufnahme über mehrere Kanäle bis hin zur Untersuchung, behördlichen Berichterstattung und Lösungsverfolgung mit vollständiger Rückverfolgbarkeit zu zugehörigen Qualitätsereignissen.
OOS-Management
OOS-Verwaltungssoftware für Untersuchungen außerhalb der Spezifikation
Strukturierte Arbeitsabläufe für die Untersuchung außerhalb der Spezifikation der Phasen I und II, ausgerichtet an den FDA-Richtlinien, mit wissenschaftlicher Genauigkeit und vollständiger behördlicher Vertretbarkeit.
OOT-Management
Out-of-Trend-Analyse
Statistische Trendüberwachung und alarmgesteuerte Untersuchungsworkflows zur Erkennung allmählicher Qualitätsänderungen, bevor sie zu OOS-Ereignissen werden, und ermöglichen so ein proaktives Qualitätsmanagement.
Management von Laborvorfällen
Software zur Verwaltung von Laborvorfällen für pharmazeutische QC-Labore
Verfolgen und untersuchen Sie Gerätefehlfunktionen, Probenkontaminationen, Umgebungsabweichungen und Analystenfehler mit strukturierten Korrekturmaßnahmen-Workflows und GxP-Konformität.
Qualitätsrisikomanagement
KI-gesteuertes Qualitätsrisikomanagementsystem
Auf ICH Q9 ausgerichtetes Risikomanagement mit FMEA, Fischgrätenanalyse, Risikobewertung, KI-gesteuerter Risikoidentifizierung und Unternehmensrisiko-Dashboards für proaktive Qualitätsentscheidungen.
Anbieter-/Lieferantenqualifikation
Software für Lieferantenqualitätsmanagement und Lieferantenqualifizierung
Durchgängiges Lieferantenlebenszyklusmanagement – von der Erstqualifizierung über die laufende Leistungsüberwachung, risikobasierte Auditplanung bis hin zur regelmäßigen Neuqualifizierung.
Produktrückrufmanagement
Initiieren, Ausführen, Melden, Schließen
Schnelle Einleitung und Durchführung von Rückrufen mit Rückverfolgbarkeit auf Chargenebene, Verwaltung behördlicher Benachrichtigungen, Verfolgung der Kundenkommunikation und Bewertung der Wirksamkeit nach dem Rückruf.
CAPA-Lebenszyklus: Wirksamkeitsprüfungen
Lebenszykluskontrolle, Beweiserfassung und Automatisierung für die Durchsetzung gesetzlicher Vorschriften
Erkennung
Identifizieren Sie Probleme aufgrund von Abweichungen, Beschwerden, Audits und OOS/OOT. Klassifiziert Ereignisse automatisch und verknüpft Quelldatensätze.
Untersuchung
Ursachenanalyse mit Zeitplänen, Datenspuren und Risikobewertung. Historische Muster leiten Untersuchungen.
Aktionsplan
Das System empfiehlt relevante Maßnahmen, Risikoprioritäten und bewährte Best Practices.
Durchführung
Führen Sie Maßnahmen durch, fügen Sie Beweise bei, aktualisieren Sie verknüpfte Abweichungen, Änderungen und Beschwerdeaufzeichnungen.
KI-Effektivitätsintelligenz
KI vergleicht jede neue CAPA mit offenen CAPAs ähnlicher Art zur Wirksamkeitsprüfung – sie weist auf Überschneidungen hin, empfiehlt eine Konsolidierung und verhindert redundante Untersuchungen.
Schließung
Bestätigen Sie Beweise, stellen Sie Links zu Audit-/Beschwerdeaufzeichnungen fertig und archivieren Sie sie zur behördlichen Überprüfung.
Erkennung
Identifizieren Sie Probleme aufgrund von Abweichungen, Beschwerden, Audits und OOS/OOT. Klassifiziert Ereignisse automatisch und verknüpft Quelldatensätze.
Untersuchung
Ursachenanalyse mit Zeitplänen, Datenspuren und Risikobewertung. Historische Muster leiten Untersuchungen.
Aktionsplan
Das System empfiehlt relevante Maßnahmen, Risikoprioritäten und bewährte Best Practices.
Durchführung
Führen Sie Maßnahmen durch, fügen Sie Beweise bei, aktualisieren Sie verknüpfte Abweichungen, Änderungen und Beschwerdeaufzeichnungen.
KI-Effektivitätsintelligenz
KI vergleicht jede neue CAPA mit offenen CAPAs ähnlicher Art zur Wirksamkeitsprüfung – sie weist auf Überschneidungen hin, empfiehlt eine Konsolidierung und verhindert redundante Untersuchungen.
Schließung
Bestätigen Sie Beweise, stellen Sie Links zu Audit-/Beschwerdeaufzeichnungen fertig und archivieren Sie sie zur behördlichen Überprüfung.
Manuelle vs. digitale Qualitätsmanagementsystem-Software
Quantifizierter ROI durch den Einsatz der cloudbasierten pharmazeutischen Qualitätsmanagementsoftware AmpleLogic über den gesamten Qualitätslebenszyklus hinweg
Abweichungsuntersuchungszyklus
35-50 % schnellerDurchschnittliche Zykluszeit von 45–90 Tagen mit papierbasierter Untersuchung, E-Mail-gesteuerter Koordination und manueller abteilungsübergreifender Beweiszusammenstellung
Automatisierte Arbeitsabläufe mit KI-gestütztem RCA, automatisch verknüpften Qualitätsdatensätzen und konfigurierbarer SLA-Verfolgung verkürzen die Zykluszeit auf 15–30 Tage
CAPA-Abschluss- und Wirksamkeitsüberprüfung
40-60 % schneller60–120-tägige CAPA-Zyklen mit manueller Nachverfolgung, verpassten Wirksamkeitsprüfungen, isolierten Aktionsplänen und keiner systematischen Beweiserfassung
Geschlossener Lebenszyklus mit automatisierten Wirksamkeitsprüfungen, Meilensteinverfolgung, Nachweisanforderungen und KI-empfohlenen Korrekturmaßnahmen
Auditvorbereitung und Inspektionsbereitschaft
80 % Aufwand eingespart2–4 Wochen manuelle Beweiszusammenstellung, systemübergreifende Querverweise und Zusammenstellung der Dokumentation in letzter Minute vor jedem Audit
Bei Bedarf generierte, inspektionsfertige Beweispakete – Audit-Trail-Erstellung mit einem Klick, Echtzeit-Compliance-Dashboards und Lückenanalyse
Lebenszyklus der Änderungskontrolle
60 % ZyklusverkürzungMehrwöchige abteilungsübergreifende Folgenabschätzungen mit manueller Genehmigungsweiterleitung, unterbrochener Implementierungsverfolgung und verzögerten SOP-Updates
KI-gestützte Vorhersage der Auswirkungen von Änderungen, automatisiertes Multi-Stakeholder-Routing, meilensteinbasierte Implementierungsverfolgung und automatisch ausgelöste SOP-/Schulungsaktualisierungen
KI-gestütztes Qualitätsmanagementsystem
Nutzen Sie KI-Agenten und maschinelles Lernen, um Untersuchungen zu automatisieren, Risiken vorherzusagen und die Entscheidungsfindung in Bezug auf Qualität auf Ihrer digitalen Qualitätsmanagementplattform zu beschleunigen
CAPA-Effektivitätsintelligenz
KI überwacht kontinuierlich offene CAPAs zur Wirksamkeitsprüfung und vergleicht automatisch jedes neue CAPA ähnlicher Art. Dabei werden potenzielle Duplikate gekennzeichnet, eine Konsolidierung oder Querverweise empfohlen und bestehende Korrekturmaßnahmen sichtbar gemacht, um überflüssige Untersuchungen zu verhindern
Qualitäts-Ereigniszusammenfassungsagenten
Sammeln Sie automatisch Daten über Untersuchungen, Abweichungen und CAPA-Pläne hinweg, um narrative Zusammenfassungen zu erstellen – und reduzieren Sie so die Dokumentationszeit um 60 %.
KI-gestützte Ursachenanalyse
Vergleichen Sie Muster mit historischen CAPA- und Abweichungsdaten, um wahrscheinliche Grundursachen vorherzusagen, bewährte vorbeugende Maßnahmen zu empfehlen und wichtige Treiber zu erklären
Prädiktive Qualitätsanalyse
Modelle für maschinelles Lernen erkennen aufkommende Qualitätssignale, prognostizieren Abweichungstrends und priorisieren Bereiche mit hohem Risiko, bevor sie zu Compliance-Problemen werden
Intelligente Vorhersage der Auswirkungen von Veränderungen
Analysieren Sie historische Änderungsdaten und Abweichungsmuster, um die Auswirkungen von Änderungen auf Produkte, Prozesse und Zulassungsanträge vor der Implementierung vorherzusagen
Automatisierte Workflow-Optimierung
KI lernt kontinuierlich aus Prozessausführungsdaten, um Workflow-Verbesserungen vorzuschlagen, Engpässe zu identifizieren und SLA-optimierte Routing-Pfade zu empfehlen
Funktionen der eQMS-Plattform
Softwarefunktionen für Qualitätsmanagementsysteme der Enterprise-Klasse – CAPA-Management, Abweichungsmanagement, Audit-Management, Nichtkonformitätsmanagement-Software und Lieferantenqualität mit integrierter Qualitäts-Workflow-Automatisierung für Life Sciences-Compliance
Überprüfung der Wirksamkeit im geschlossenen Regelkreis
Integrierte Verifizierungsworkflows für CAPA, Änderungskontrolle, Abweichungen und Audits – mit vordefinierten Erfolgskriterien, Wiederholungstestprotokollen und automatisierter Beweiszusammenstellung für die behördliche Verteidigung.
Risikobasierte Entscheidungsunterstützung
Harmonisierung der Qualität an mehreren Standorten
Qualitäts-Dashboards in Echtzeit
Elektronische Signatur und Audit Trail
Konfigurierbare Low-Code-Workflow-Engine
KI-gestützte Ermittlungsunterstützung
Jährliche Überprüfung der Produktqualität (APQR)
Mobile Qualitätsausführung
Automatisierte Eskalations-Engine
Externe Zusammenarbeit in Echtzeit
Bringen Sie interne Teams, CDMOs, Lieferanten und Partner in ein einziges Qualitätsökosystem für schnellere Lösungen und globale Ausrichtung
Lieferanten- und CDMO-Zugriff
Gewähren Sie externen Partnern kontrollierten Zugriff für die Zusammenarbeit in Echtzeit bei Untersuchungen, Auditergebnissen und Korrekturmaßnahmen von Lieferanten
Auftragslaborkoordination
Teilen Sie OOS/OOT-Daten, koordinieren Sie Untersuchungen und verwalten Sie Methodentransfers mit Vertragstestlaboren in einem einheitlichen System
Bereitschaft der Aufsichtsbehörden
Generieren Sie mit einem Klick prüfbereite Beweispakete – vollständige Prüfprotokolle, verknüpfte Qualitätsaufzeichnungen und Compliance-Dashboards
Qualitätsausrichtung an mehreren Standorten
Standardisieren Sie Qualitätsprozesse an globalen Produktionsstandorten mit zentraler Konfiguration, lokalisierten Arbeitsabläufen und konsolidiertem Reporting
Einheitlicher eQMS-Integrationshub
Cloudbasierte QMS-Software, die nahtlos mit Ihrem gesamten Unternehmensökosystem verbunden ist und eine durchgängige Rückverfolgbarkeit der Qualität gewährleistet
Dokumentenmanagement (DMS)
SOP-Revisionen, kontrollierte Kopieverteilung, Versionsverwaltung
Lernmanagement (LMS)
Automatisch ausgelöste Schulung zu Änderungskontrollgenehmigungen und SOP-Updates
LIMS
Laborvorfälle, Abweichungen, automatische OOS/OOT-Initiierung und Datenabruf
eBMR / MES
Auslöser für Chargensperre, Erfassung von Produktionsabweichungen, Prozessdaten in Echtzeit
Regulatorisch (RIMS)
Koordinierung der Änderungskontrolle, Auswirkungen der Produktregistrierung, behördliche Einreichungen
Reinigungsvalidierung
Abweichungen, OOS/OOT von Reinigungsprozessüberwachung und Grenzwertprüfung
eLogbuch
Abweichungserfassung von Logbuchereignissen, Umweltausflügen
Sicherheit / Pharmakovigilanz
Verknüpfung von Beschwerde und Sicherheitsfall, Korrelation unerwünschter Ereignisse
ERP / Lieferkette
Synchronisierung von Lieferantendaten, Chargengenealogie, Materialrückverfolgbarkeit, Lagerverwaltung

AmpleLogic eQMS Hub
Vernetztes Unternehmensökosystem
GxP-konformes Qualitätsmanagementsystem
FDA 21 CFR Part 11-konformes QMS, ISO 13485-Qualitätsmanagementsystem und GMP-Qualitätsmanagementsoftware mit integrierter Audit-Bereitschaftssoftware, Inspektionsbereitschaftsplattform und Pharma-Compliance-Management für reguliertes Branchenqualitätsmanagement
21 CFR Teil 11
Elektronische Aufzeichnungen und Signaturen
EU-Anhang 11
Validierung computergestützter Systeme
ICH Q9
Qualitätsrisikomanagement
ICH Q10
Pharmazeutisches Qualitätssystem
GAMP 5 / ISPE
Risikobasierte Validierung
ISO 9001/13485
Qualitäts- und Medizinproduktestandards
EU-MDR/IVDR
Verordnung über Medizinprodukte
ALCOA+-Prinzipien
Datenintegritätsrahmen
Qualitätsmanagement-Software für jedes Life-Science-Segment
Branchenspezifische eQMS-Lösungen – pharmazeutisches Qualitätsmanagementsystem, Biotech-QMS-Software und Medizingeräte-QMS-Software für jeden regulierten Hersteller
Pharmazeutisch
End-to-End-GMP-Qualitätsmanagementsoftware für Arzneimittelherstellung, API-Produktion und Formulierungsanlagen – speziell entwickelte Qualitätsmanagementsoftware für die Pharmaindustrie.
Biotechnologie
Spezialisierte Qualitätsmanagementsoftware für die Biotechnologie – zur Unterstützung der Entwicklung und Herstellung von Biologika, Biosimilars und fortschrittlichen Therapien.
Medizinische Geräte
Qualitätsmanagementsoftware für medizinische Geräte – ISO 13485, EU MDR/IVDR-konform für Gerätedesign, Herstellung und Überwachung nach dem Inverkehrbringen.
Gen- und Zelltherapie
Qualitätsmanagementsystem für die Biowissenschaften für die Herstellung von ATMP und Zell-/Gentherapie mit spezieller regulatorischer Ausrichtung.
CDMO / CMO
Enterprise-Qualitätsmanagementsystem für Auftragsfertiger mit Mandantenqualitätsmanagement und Auditbereitschaft.
Nutrazeutika
Pharmazeutische Qualitätsmanagementsoftware für die Herstellung von Nahrungsergänzungsmitteln und Nutrazeutika mit GMP-Konformität.
AmpleLogic eQMS – Pharmazeutische Qualitätsmanagementsoftware
Beschleunigen Sie das Pharma-Compliance-Management, die Untersuchungen, die Verifizierung und die Auditbereitschaft über den gesamten Qualitätslebenszyklus hinweg mit QMS-Lösungen für Unternehmen und Compliance-Software für die Biowissenschaften
GxP-konformes Qualitätsmanagementsystem mit FDA, ICH Q10, ISO, EU MDR/IVDR und WHO GMP-Abdeckung
40–50 % schnellere Untersuchungen und CAPA-Abschlüsse mit KI-gestützten Funktionen des Qualitätsmanagementsystems
Nachweisbare Wirksamkeitsüberprüfung im geschlossenen Regelkreis in jeder Phase des QMS-Lebenszyklus
Auditbereite Beweiszusammenstellung innerhalb von Sekunden – nicht Tagen – für das Pharma-Compliance-Management
Pilot-First-Rollout mit risikobasierter Validierung (GAMP 5 ausgerichtet) auf cloudbasierter QMS-Software
Externe Zusammenarbeit in Echtzeit mit CDMOs, Lieferanten und Partnern über Lieferantenqualitätsmanagementsoftware
Globale Qualitätsausrichtung an mehreren Standorten und in mehreren Sprachen vom ersten Tag an mit dem unternehmensweiten Qualitätsmanagementsystem
Einheitliche Qualitätsdaten für Annual Product Quality Reviews (APQR) in einer einzigen digitalen Qualitätsmanagementplattform
eQMS-Auszeichnungen für Softwareanerkennung und Kundenzufriedenheit
Führende Life-Science-Organisationen weltweit vertrauen darauf
Nr. 1: Am einfachsten zu verwenden
Medizinisches QMS
Höchste Kundenzufriedenheit
Branchenführender CSAT
Stärken der Plattform
Anpassung per Drag-and-Drop
89 G2-Abzeichen
Führend in mehreren Kategorien
"Das QMS-System von Amplelogic verfügt über alle erforderlichen qualitätsbezogenen Module und alle Abweichungen, Änderungskontrollen und CAPAs werden effektiv verwaltet und verfolgt. Alle Module sind super einfach zu bedienen."
Kandikattu K.
Qualitätsprofi
"Es lässt sich nahtlos in unsere anderen Tools integrieren. Sie haben die meisten unserer individuellen Anpassungswünsche berücksichtigt und es für uns sehr benutzerfreundlich gemacht."
Qualitätssicherungsmanager
Mittelständische Pharmaindustrie
"Das System entspricht den Anforderungen von 21 CFR Part 11 und EU Annex 11. Die Unterstützung durch das Team bei der Ersteinrichtung war wirklich hilfreich und hat den Übergang reibungslos gestaltet."
Krishna C.
Compliance-Leiter
Sind Sie bereit, Ihr Qualitätsmanagementsystem zu transformieren?
Schließen Sie sich führenden Pharma-, Biotech- und Medizingeräteunternehmen an und beschleunigen Sie die Compliance mit dem besten elektronischen Qualitätsmanagementsystem (eQMS) – einer cloudbasierten digitalen QMS-Plattform und einer SaaS-QMS-Plattform für das moderne Unternehmen.
Bleiben Sie in den Biowissenschaften an der Spitze
Erhalten Sie die neuesten Produktaktualisierungen, Compliance-News und Brancheneinblicke in Ihren Posteingang.