مؤسسة مدعومة بالذكاء الاصطناعي حلول لكل سير عمل فارما
مجموعة شاملة من الحلول البرمجية المعتمدة للمؤسسات الصيدلانية والتكنولوجيا الحيوية وعلوم الحياة.
aPaaS ذو الكود المنخفض لعلوم الحياة — العمارة التكاملية الموحدة
لا تعمل وحدات AmpleLogic في عزلة. كل حل مترابط - مشاركة البيانات، وبدء سير العمل، والحفاظ على مصدر واحد للحقيقة عبر وظائف مختبر الجودة والتصنيع ومراقبة الجودة.
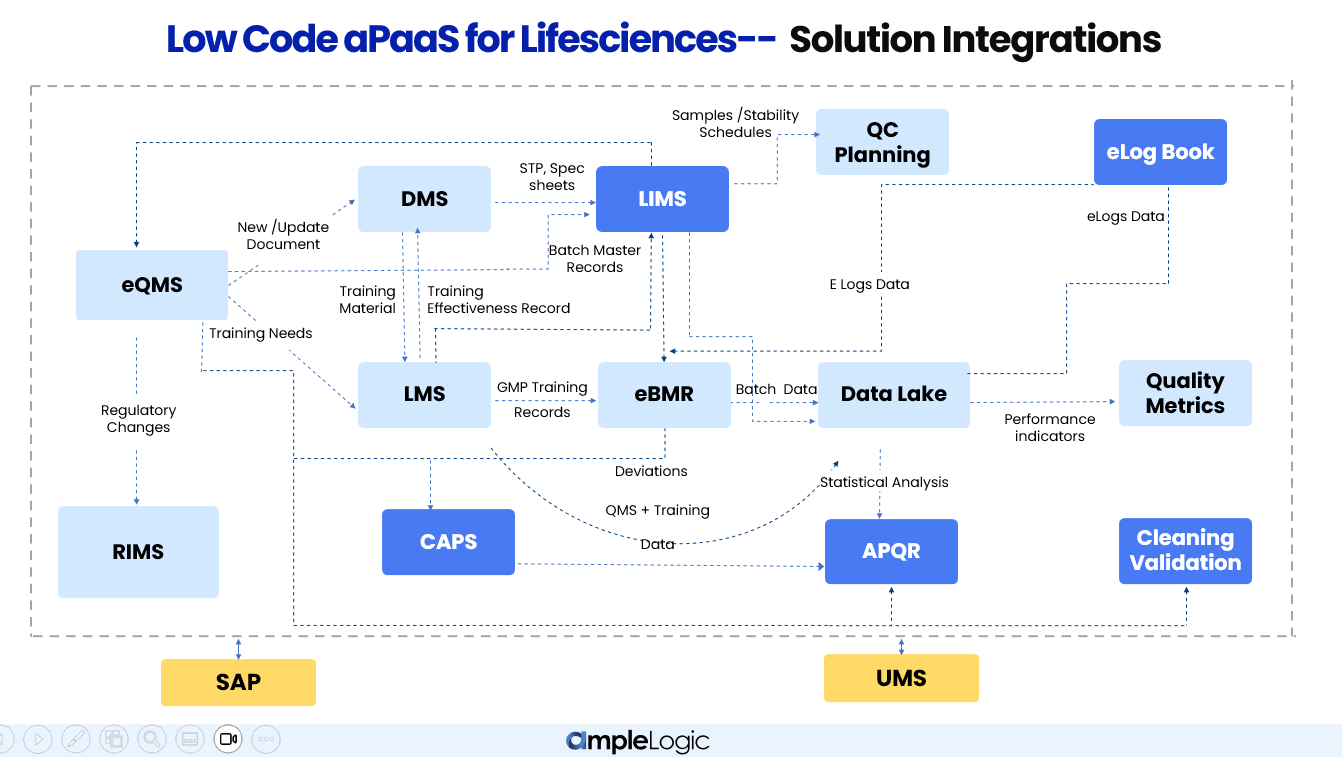
كيف تتكامل وحدات AmpleLogic عبر وظائف الجودة والتصنيع ومراقبة الجودة في شركات الأدوية
بحيرة البيانات الموحدة
تتغذى جميع الوحدات في بحيرة بيانات مركزية، مما يتيح مؤشرات الأداء في الوقت الفعلي، ومقاييس الجودة، والتحليلات متعددة الوظائف دون الحاجة إلى توحيد البيانات يدويًا.
سلاسل سير العمل الآلية
يؤدي حدث واحد - مثل الانحراف في التصنيع - إلى تشغيل CAPA تلقائيًا في نظام إدارة الجودة الإلكترونية، ومراجعة المستندات في DMS، وإعادة التدريب في LMS، وتقييم التأثير في APQR.
تدفق البيانات ثنائي الاتجاه
تتدفق البيانات في كلا الاتجاهين بين الوحدات. على سبيل المثال، يرسل LMS سجلات فعالية التدريب مرة أخرى إلى eQMS، ويعيد LIMS النتائج التحليلية إلى eBMR لإصدار الدُفعات.
كيف تعمل عمليات التكامل عبر الوظائف
إدارة الجودة
يضمن النظام البيئي لإدارة الجودة تتبع كل انحراف، وCAPA، والتحكم في التغيير، ونتائج التدقيق من البداية إلى النهاية. يقع نظام إدارة الجودة الإلكترونية (eQMS) في المركز - مما يؤدي إلى تشغيل سير عمل المستندات في DMS، ومهام التدريب في نظام إدارة التعلم (LMS)، وتغذية البيانات الإحصائية في APQR لإجراء مراجعات جودة المنتج السنوية.
وثيقة جديدة / تحديث
عند ظهور انحراف أو تحكم في التغيير في نظام إدارة الجودة الإلكترونية، يبدأ نظام إدارة الجودة تلقائيًا سير عمل مراجعة إجراءات التشغيل القياسية (SOP)، مما يضمن بقاء المستندات محدثة مع كل حدث جودة.
الاحتياجات التدريبية
تؤدي إجراءات التشغيل المعيارية (SOP) الجديدة أو المنقحة إلى تشغيل مهام التدريب التلقائي في نظام إدارة التعلم (LMS). تتدفق سجلات فعالية التدريب مرة أخرى إلى نظام إدارة الجودة الإلكترونية لإغلاق حلقة الجودة.
التحليل الإحصائي
يتم تجميع البيانات المجمعة والانحرافات وسجلات CAPA ومعلمات العملية في Data Lake وإدخالها في APQR لإجراء مراجعات سنوية شاملة لجودة المنتج.
نظام إدارة الجودة + بيانات التدريب
تتدفق انحرافات المعايرة وسجلات الصيانة الوقائية من CAPS إلى APQR، مما يوفر صورة كاملة عن تأثير المعدات والأدوات على جودة المنتج.
البقاء متقدما في علوم الحياة
احصل على آخر تحديثات المنتج وأخبار الامتثال ورؤى الصناعة التي يتم تسليمها إلى صندوق الوارد الخاص بك.