تتبع كل تقديم وتسجيل على مستوى العالم
نظام إدارة معلومات تنظيمية مصمم خصيصًا للمستحضرات الصيدلانية - أتمتة عمليات التقديم وتتبع ملفات ANDA وDMF وإدارة دورات حياة منتجات الأدوية عبر أكثر من 120 دولة باستخدام برنامج الامتثال التنظيمي المدعوم بالذكاء الاصطناعي.
120+
البلدان المدعومة
50%
تقديمات أسرع
100%
جاهز للتدقيق
24/7
مراقبة الامتثال
تحديات RIMS: لماذا تفشل الإدارة التنظيمية اليدوية؟
التحديات الحاسمة التي تعيق الامتثال والتقديمات والوصول إلى الأسواق
اللوائح العالمية المتطورة باستمرار
إن مواكبة إدارة الغذاء والدواء (FDA)، ووكالة الأدوية الأوروبية (EMA)، وMHRA، وCDSCO، ومنظمة الصحة العالمية، ووزارة الصحة الكندية، وTGA، وأكثر من 100 سلطة إقليمية تتطلب يقظة مستمرة وتكيفًا سريعًا.
البيانات التنظيمية المجزأة
تؤدي المعلومات التنظيمية الهامة المنتشرة عبر رسائل البريد الإلكتروني وجداول البيانات ومحركات الأقراص المشتركة والأنظمة القديمة إلى إنشاء نقاط عمياء وفجوات في الامتثال.
تنسيقات التقديم المعقدة
تتطلب إدارة eCTD وACTD وNeeS والطلبات الورقية عبر مناطق مختلفة خبرة متخصصة وتنسيقًا يدويًا معرضًا للأخطاء.
ضعف الرؤية والتتبع
لا توجد لوحة تحكم موحدة للحالة في الوقت الفعلي لعمليات التقديم والموافقات والاستعلامات والجداول الزمنية للتجديد عبر الأسواق.
العمليات اليدوية والمعرضة للخطأ
يؤدي الاعتماد الكبير على التواصل عبر البريد الإلكتروني، وإدخال البيانات يدويًا، وجداول البيانات المنفصلة إلى زيادة خطر فقدان المواعيد النهائية والعقوبات التنظيمية.
تحديات التكامل
تتسبب أنظمة QMS وDMS وERP وأنظمة السلامة المنفصلة في ازدواجية البيانات وعدم الاتساق وبطء سير العمل التنظيمي متعدد الوظائف.
قضايا قابلية التوسع
يؤدي تزايد مجموعات المنتجات عبر المناطق الجغرافية إلى زيادة التعقيد التنظيمي بشكل كبير، مما يؤدي إلى إرباك أساليب التتبع اليدوي.
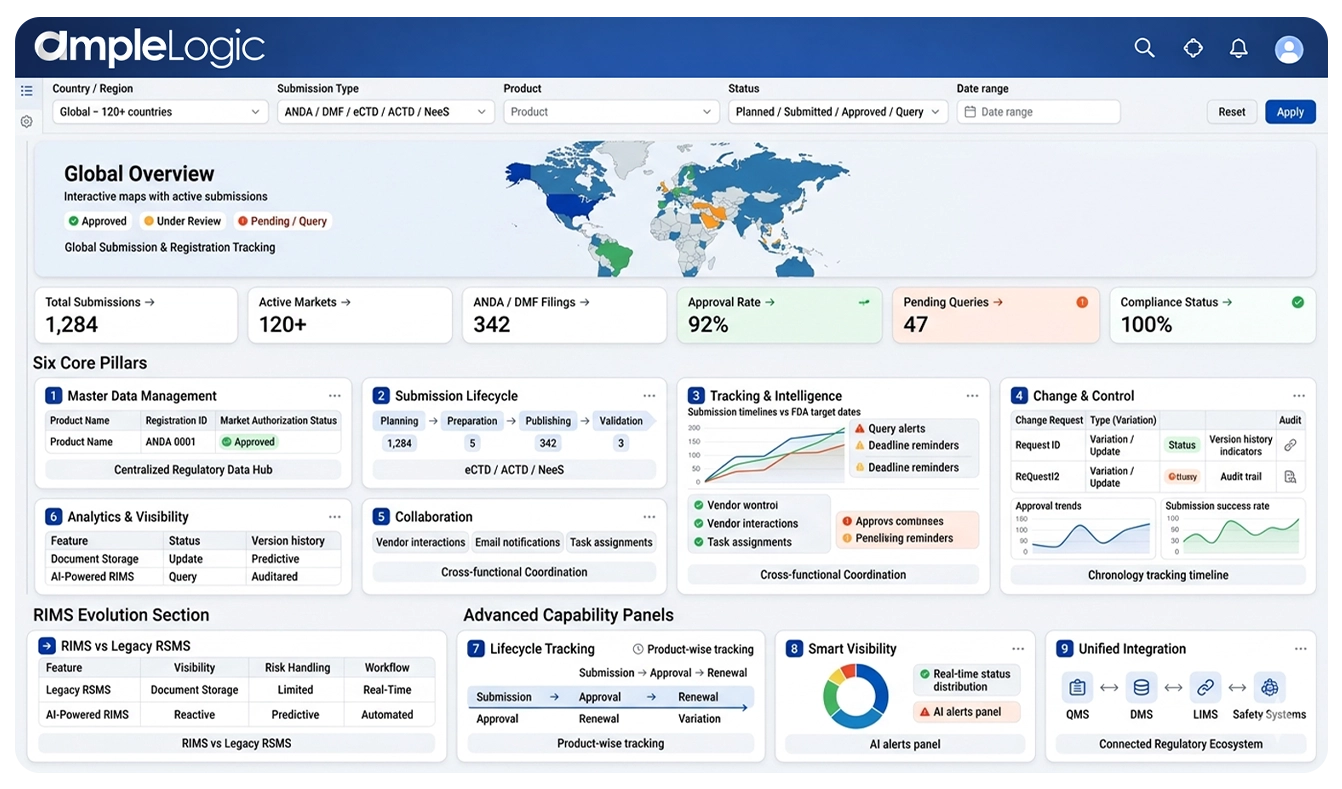
نظرة عامة على برنامج AmpleLogic RIMS
ست ركائز تمكن من إدارة دورة الحياة التنظيمية الشاملة
إدارة البيانات الرئيسية
التسجيل المركزي للمنتج، وترخيص السوق العالمية، وتتبع دورة الحياة عبر جميع السلطات التنظيمية.
دورة حياة التقديم
سير العمل الآلي للتخطيط والإعداد والنشر والتحقق من صحة عمليات إرسال eCTD وACTD وNeeS مع تتبع ANDA وDMF.
التتبع والاستخبارات
حالة التقديم في الوقت الفعلي، وإدارة الموافقة والاستعلام، والتواريخ المستهدفة لإدارة الغذاء والدواء الأمريكية (FDA)، والمراقبة الاستباقية للمواعيد النهائية في جميع الأسواق.
التغيير والتحكم
التحكم في التغيير وإدارة الاختلافات وعملية التحسين المستمر (CIP) مع مسارات التدقيق الكاملة وسجل الإصدارات.
تعاون
التنسيق بين الموردين، وإخطار العملاء، وتنبيهات البريد الإلكتروني الآلية لسير العمل التنظيمي السلس متعدد الوظائف.
التحليلات والرؤية
لوحات المعلومات الرسومية، وتتبع التسلسل الزمني، وتحليلات دورة الحياة، والمعلومات الجاهزة للامتثال لاتخاذ قرارات تنظيمية مستنيرة.
RIMS: التطور التالي لـ RSMS
في حين كانت منصات RSMS القديمة عبارة عن مخازن مستندات سلبية، فإن RIMS عبارة عن نظام بيئي ذكي للإدارة التنظيمية مدعوم بالذكاء الاصطناعي يعمل بشكل فعال على دفع الامتثال والتنبؤ بالمخاطر وتسريع وقت طرح المنتج في السوق.
إدارة البيانات
التسجيل الكامل للمنتج والبيانات التنظيمية العالمية في نظام مركزي مع إدارة البيانات الرئيسية وتتبع دورة الحياة.
تتبع دورة الحياة
مراقبة الموافقات والتغييرات والتجديدات لضمان الامتثال التنظيمي المستمر في جميع الأسواق.
الرؤية الذكية
رؤية عالمية في الوقت الفعلي ومراقبة استباقية من خلال التنبيهات الذكية ولوحات معلومات الامتثال.
التكامل الموحد
التكامل السلس مع أنظمة QMS وDMS وLIMS وأنظمة السلامة لبناء نظام بيئي موحد للإدارة التنظيمية.
وحدات سير عمل RIMS: إدارة دورة حياة التقديم
ثماني وحدات مترابطة توجه العمليات التنظيمية من الاستراتيجية إلى الامتثال المستمر
مؤسسة البيانات التنظيمية
إعداد السوق العالمية ومستودع البيانات الرئيسية لـ DMF وCEP وLOA وتتبع دورة حياة المنتج عبر جميع السلطات.
تخطيط التقديم
تطوير الإستراتيجية، وإدارة الجدول الزمني، وتتبع المعالم، وتخصيص الموارد لتقديم الطلبات التنظيمية العالمية.
إعداد التقديم
تجميع الملفات والتحكم في الإصدار وتجميع المستندات من أجل جاهزية eCTD / ACTD / NeeS من خلال عمليات التحقق من الصحة الآلية.
تنفيذ التقديم
التحقق من الصحة، والنشر للسلطات الصحية، وتقديم البوابة، وتتبع ANDA، ومراقبة حالة السلطة في الوقت الفعلي.
إدارة المراجعة
تتبع الاستعلام وإدارة النقص وسجلات اتصالات السلطة ومراقبة الجدول الزمني للاستجابة في جميع الأسواق.
إدارة دورة حياة المنتج الدوائي
الاختلافات والتجديدات وتغييرات ما بعد الموافقة وتحديثات التصنيفات مع تتبع دورة الحياة الكاملة والتنبيهات التلقائية.
مراقبة الامتثال
التنبيهات التلقائية، وتتبع الالتزام، والاستعداد للتفتيش، ومعلومات استباقية بشأن التغيير التنظيمي.
التحليلات وإعداد التقارير
لوحات المعلومات في الوقت الفعلي، والتقارير الرسومية، ورؤى التقديم العالمية، والتحليلات الخاصة بـ GDUFA/السلطة.

التنسيق من النهاية إلى النهاية
تتكامل كل وحدة من وحدات سير العمل بسلاسة مع أنظمة QMS وDMS وLIMS وأنظمة السلامة، مما يؤدي إلى التخلص من صوامع البيانات وعمليات التسليم اليدوية عبر دورة الحياة التنظيمية بأكملها.
الميزات الرئيسية لبرنامج AmpleLogic RIMS
اثنتا عشرة قدرة حاسمة تمكن من التميز التنظيمي
تتبع تسجيل المنتج
تتبع تسجيلات المنتجات في أكثر من 120 دولة من خلال تحديثات الحالة التلقائية وتنبيهات المواعيد النهائية وإدارة دورة حياة المنتج الدوائي الكاملة.
إعداد التقديم والنشر
مراقبة الموافقة والرفض
ANDA Tracker والتواريخ المستهدفة لإدارة الغذاء والدواء
تعقب DMF والتحكم في التغيير
إدارة الالتزام والتنوع
إدارة البائعين وأصحاب المصلحة
التقارير الرسومية ولوحات المعلومات
سير العمل التنظيمي الدوائي الآلي
التوقيعات الإلكترونية ومسارات التدقيق
مستودع الوثائق المركزي
محرك التحقق من صحة التقديم
RIMS مدعومة بالذكاء الاصطناعي: التحليلات التنظيمية الذكية
تعمل ست إمكانات مدعومة بالذكاء الاصطناعي على تسريع سير العمل التنظيمي وتقليل المخاطر
تتبع الامتثال لمنظمة العفو الدولية
المراقبة المستمرة والتكيف مع المعايير التنظيمية المحلية والعالمية المتطورة، وتحديث العمليات تلقائيًا لضمان الامتثال دون تدخل يدوي.
التحليلات التنبؤية
يحلل البيانات التاريخية وفي الوقت الفعلي لتحديد المخاطر المحتملة وفجوات الامتثال قبل تفاقمها، مما يساعد بشكل استباقي على تخفيف المشكلات وتجنب العقوبات.
التقارير الآلية
يقوم الذكاء الاصطناعي بأتمتة عملية إنشاء التقارير والوثائق التنظيمية، مما يضمن دقتها وفي الوقت المناسب وجاهزيتها للتدقيق مع الحد الأدنى من المشاركة البشرية.
محرك تخفيف المخاطر
تقوم الخوارزميات المدعومة بالذكاء الاصطناعي بتقييم أنماط البيانات لتحديد مخاطر الامتثال المحتملة، وتقديم رؤى تنبؤية والتوصية بالإجراءات التصحيحية.
استخبارات التغيير التنظيمي
يتتبع ويعالج التغييرات التنظيمية في الوقت الفعلي، وينفذها تلقائيًا في أنظمتك لضمان الامتثال المستمر لأحدث المعايير.
تحسين سير العمل
يعمل الذكاء الاصطناعي على تحسين سير العمل، وتقليل تكاليف التشغيل، وتسريع العمليات التنظيمية، وضمان الامتثال المتسق عبر جميع مستويات الأعمال.
أجهزة التتبع التنظيمية العالمية: مراقبة إدارة الغذاء والدواء الأمريكية وEMA وRoW
ثلاث وحدات تتبع إقليمية للحصول على ترخيص شامل للسوق
الولايات المتحدة الأمريكية FDA التنظيمية المقتفي
متعقب ANDA ومتعقب DMF مع معالم دورة حياة إدارة الغذاء والدواء بما في ذلك IND وNDA وANDA وتواريخ الإجراءات المستهدفة BLA ورسوم GDUFA وعمليات التقديم 505(ب)(2).
المتتبع التنظيمي للاتحاد الأوروبي والمملكة المتحدة
إدارة إجراءات EMA وMHRA، واختلافات الاعتراف المركزي/اللامركزي/المتبادل، وجداول PSUR، وتقديمات المملكة المتحدة بعد خروج بريطانيا من الاتحاد الأوروبي مع سير العمل الآلي.
المتتبع التنظيمي للصف العالمي
قم بتبسيط عمليات التقديم في منطقة آسيا والمحيط الهادئ، وأمريكا اللاتينية، ومنطقة الشرق الأوسط وشمال أفريقيا، وأفريقيا من خلال تتبع دورة الحياة الخاصة بكل بلد لـ Health Canada، وTGA، وCDSCO، وWHO PQ، وأكثر من 100 هيئة.
الامتثال لـ RIMS: المعايير التنظيمية العالمية
الدعم الكامل للأطر التنظيمية العالمية ومعايير الامتثال
دعم السلطة الرئيسية
تغطية كاملة لـ US FDA، وEMA، وMHRA، وWHO، وHealth Canada، وTGA، وCDSCO، وANVISA، وPMDA، وأكثر من 100 هيئة صحية عالمية.
إدارة التنسيق متعدد المناطق
الدعم الأصلي لـ eCTD وACTD وNeeS والتنسيقات الورقية مع مراقبة التجديد الآلي والتحقق من صحة التنسيق.
21 CFR الجزء 11 وملحق الاتحاد الأوروبي 11
ضوابط متوافقة تمامًا بما في ذلك التوقيعات الإلكترونية ومسارات التدقيق وضمانات سلامة البيانات والتحكم الآمن في الإصدار.
المراقبة والتنبيهات الاستباقية
تنبيهات تلقائية للمواعيد النهائية وتواريخ استحقاق الالتزام وفترات التجديد والتغييرات التنظيمية مع تقليل المخاطر في الوقت الفعلي.
جاهزية IDMP
يدعم معايير ISO IDMP للمادة والمنتج والتنظيم والبيانات المرجعية للتحضير لمتطلبات تعريف EMA.
ICH eCTD 4.0 جاهز
مُثبت للمستقبل بالنسبة لنموذج بيانات eCTD 4.0 من الجيل التالي مع تخطيط المحتوى المنظم وإدارة البيانات الوصفية وإمكانيات تقديم السلطة.
AmpleLogic RIMS مقابل المنافسين
كيف يتفوق AmpleLogic على RIMS القديمة وحلول النقاط
| القدرة | إطارات AmpleLogic | المنافسين |
|---|---|---|
| بنيان | كود منخفض / بدون كود على aPaaS الموحد | بنية صلبة، هناك حاجة إلى تخصيص كبير |
| نهج البيانات | مستودع البيانات الرئيسية الموحد | بيانات مجزأة عبر الوحدات والصوامع |
| تغطية دورة الحياة | من البداية إلى النهاية (التخطيط لتتبع ما بعد الموافقة) | غالبًا ما يتطلب الأمر وحدات إضافية منفصلة |
| اندماج | سلس (QMS، DMS، ERP، السلامة، LIMS) | مستقلة، وتكلفة التكامل العالية والجهد |
| الأتمتة والذكاء الاصطناعي | تنبيهات مدعومة بالذكاء الاصطناعي، وتحليلات تنبؤية، وتقارير تلقائية | أتمتة محدودة، وسير عمل يدوي ثابت |
| التكلفة الإجمالية للملكية | انخفاض التكلفة الإجمالية للملكية، والنشر السريع، والدفع حسب النمو | رسوم الترخيص مرتفعة وتكاليف الصيانة المستمرة |
| سرعة النشر | أسابيع مع قوالب تم التحقق من صحتها مسبقًا | أشهر إلى سنوات التنفيذ |
| جاهزية eCTD 4.0 | مُثبتة للمستقبل باستخدام نموذج البيانات المنظمة | يعتمد على خارطة الطريق، وجدول زمني غير مؤكد |
تكاملات RIMS للمؤسسات
عشر وحدات تكامل تربط الأنظمة التنظيمية والجودة والتصنيع
نظام إدارة الجودة الإلكترونية
التحكم في التغيير ثنائي الاتجاه، CAPA، وربط الانحراف
نظام إدارة الوجهات السياحية
الوثائق التنظيمية وإجراءات التشغيل الموحدة (SOP) التي يتم التحكم فيها بالإصدار
نظام إدارة التعلم
سجلات التدريب وإدارة الكفاءات
ليمس
البيانات التحليلية وتكامل CoA لعمليات التقديم
سجل إلكتروني
بيانات سجل GxP مرتبطة بالسجلات التنظيمية
إي بي إم آر/ميس
بيانات السجل الدفعي لعمليات التقديم التنظيمية
CVS
تنظيف بيانات التحقق من صحة الملفات التنظيمية
أحرف استهلالية
سجلات معايرة المعدات للامتثال
ساب / أوراكل
مزامنة البيانات الرئيسية للمواد وسلسلة التوريد
الكهروضوئية
بيانات الأحداث الضارة وتكامل PSUR/PBRER
RIMS ROI: تأثير تنظيمي قابل للقياس
التأثير الكمي من إدارة دورة الحياة التنظيمية بمساعدة الذكاء الاصطناعي
إعداد التقديم
أسرع بنسبة 50-60%عملية يدوية
8-12 أسبوع
مع حواف AmpleLogic
3-5 أسابيع
إدخال البيانات التنظيمية
تخفيض 75%عملية يدوية
40+ ساعة / أسبوع
مع حواف AmpleLogic
8-10 ساعات/أسبوع
الالتزام بالموعد النهائي
المواعيد النهائية الضائعة قريبة من الصفرعملية يدوية
85-90% في الوقت المحدد
مع حواف AmpleLogic
99%+ في الوقت المحدد
وقت الاستجابة للاستعلام
استجابة أسرع بنسبة 70%عملية يدوية
5-10 أيام عمل
مع حواف AmpleLogic
1-3 أيام عمل
إعداد التدقيق
توفير الوقت بنسبة 90%عملية يدوية
2-4 أسابيع
مع حواف AmpleLogic
ساعات (جاهزة دائمًا)
إنشاء التقرير
أسرع بنسبة 95%عملية يدوية
3-5 أيام لكل تقرير
مع حواف AmpleLogic
الدقائق (يتم إنشاؤها تلقائيًا)
ظهرت في تقرير جارتنر
تم الاعتراف بشركة AmpleLogic RIMS كمورد تمثيلي في دليل السوق Gartner® لحلول إدارة المعلومات التنظيمية لعلوم الحياة، سبتمبر 2024 (المعرف G00769345).
الصناعات التي تخدمها AmpleLogic RIMS
ثمانية قطاعات صناعية تستفيد من نظام AmpleLogic RIMS لتحقيق التميز التنظيمي
المستحضرات الصيدلانية
برنامج تنظيمي متوافق مع GMP لتسجيل الأدوية، وتقديمات NDA/ANDA، وترخيص السوق العالمية مع إدارة دورة الحياة الكاملة
التكنولوجيا الحيوية
تقديمات BLA وتسجيلات البدائل الحيوية وإدارة دورة حياة المنتج البيولوجي المعقدة
الأجهزة الطبية
510(ك)، PMA، علامة CE، عمليات تقديم EUDAMED/UDI، وإدارة تصنيف الأجهزة
العلاج الجيني
طلبات IND/BLA للعلاجات المتقدمة مع تتبع المسار التنظيمي المتخصص
الشركات المصنعة لواجهة برمجة التطبيقات
متعقب DMF لتطبيقات CEP وتسجيل واجهة برمجة التطبيقات العالمية عبر السلطات
الأطعمة والمشروبات
تسجيلات المضافات الغذائية، والتطبيقات الغذائية الجديدة، وتقديم المطالبات الصحية
القنب والتبغ
التتبع التنظيمي المتخصص لترخيص القنب وتقديم منتجات التبغ
مستحضرات التجميل
إشعارات منتجات مستحضرات التجميل، وتسجيلات CPNP/FDA، وتتبع امتثال المكونات
هل أنت مستعد لتحويل عملياتك التنظيمية؟
استبدل جداول البيانات المجزأة والتتبع اليدوي بذكاء تنظيمي مدعوم بالذكاء الاصطناعي وجاهز للتدقيق.
البقاء متقدما في علوم الحياة
احصل على آخر تحديثات المنتج وأخبار الامتثال ورؤى الصناعة التي يتم تسليمها إلى صندوق الوارد الخاص بك.